As massas molares dos elementos Cu e S são, respectivamente, iguais a 63,5 g/mol e 32 g/mol.
CANTO, E. L. Minerais, minérios, metais: de onde vêm?, para onde vão? São Paulo: Moderna, 1996 (adaptado).

Creado por: juanbacan
Você também pode:
O cobre presente nos fios elétricos e instrumentos musicais é obtido a partir da ustulação do minério calcosita (Cu2S). Durante esse processo, ocorre o aquecimento desse sulfeto na presença de oxigênio, de forma que o cobre fique “livre” e o enxofre se combine com o O2 produzindo SO2, conforme a equação química:
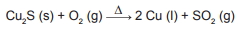
As massas molares dos elementos Cu e S são, respectivamente, iguais a 63,5 g/mol e 32 g/mol.
CANTO, E. L. Minerais, minérios, metais: de onde vêm?, para onde vão? São Paulo: Moderna, 1996 (adaptado).
Considerando que se queira obter 16 mols do metal em uma reação cujo rendimento é de 80%, a massa, em gramas, do minério necessária para obtenção do cobre é igual a:
955.
1018.
1590.
2035.
3180.
Sais de amônio são sólidos iônicos com alto ponto de fusão, muito mais solúveis em água que as aminas originais e ligeiramente solúveis em solventes orgânicos apolares, sendo compostos convenientes para serem usados em xaropes e medicamentos injetáveis. Um exemplo é a efedrina, que funde a 79 °C, tem um odor desagradável e oxida na presença do ar atmosférico formando produtos indesejáveis. O cloridrato de efedrina funde a 217 °C, não se oxida e é inodoro, sendo o ideal para compor os medicamentos.
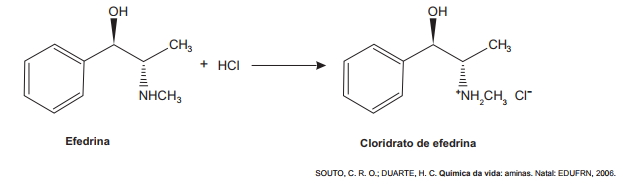
De acordo com o texto, que propriedade química das aminas possibilita a formação de sais de amônio estáveis, facilitando a manipulação de princípios ativos?
Acidez.
Basicidade.
Solubilidade.
Volatilidade.
Aromaticidade.
Considerando um combustível com 20% de adulterante, a mistura em que a adulteração seria identificada visualmente é:
etanol e água.
etanol e acetona.
gasolina e água.
gasolina e benzeno.
gasolina e querosene.
Com base nessa simulação, verifica-se que o nível da água no recipiente
subirá com a introdução do bloquinho de gelo e, após o derretimento total do gelo, esse nível subirá ainda mais.
subirá com a introdução do bloquinho de gelo e, após o derretimento total do gelo, esse nível descerá, voltando ao seu valor inicial.
subirá com a introdução do bloquinho de gelo e, após o derretimento total do gelo, esse nível permanecerá sem alteração.
não sofrerá alteração com a introdução do bloquinho de gelo, porém, após seu derretimento, o nível subirá devido a um aumento em torno de 10% no volume de água.
subirá em torno de 90% do seu valor inicial com a introdução do bloquinho de gelo e, após seu derretimento, o nível descerá apenas 10% do valor inicial.
Se essa lâmpada for ligada na rede de 110 V, o que acontecerá?
A lâmpada brilhará normalmente, mas como a tensão é a metade da prevista, a corrente elétrica será o dobro da normal, pois a potência elétrica é o produto de tensão pela corrente.
A lâmpada não acenderá, pois ela é feita para trabalhar apenas com tensão de 220 V, e não funciona com tensão abaixo desta.
A lâmpada irá acender dissipando uma potência de 50 W, pois como a tensão é metade da esperada, a potência também será reduzida à metade.
A lâmpada irá brilhar fracamente, pois com a metade da tensão nominal, a corrente elétrica também será menor e a potência dissipada será menos da metade da nominal.
A lâmpada queimará, pois como a tensão é menor do que a esperada, a corrente será maior, ultrapassando a corrente pela qual o filamento foi projetado.